Si tratta dell’Aspergillus flavus ed è studiato dall’Università della Pennsylvania. Redazione Scienza – Un team di ricercatori ha trasformato alcune molecole del fungo Aspergillus flavus in un potente composto contro il cancro. L’Aspergillus flavus è un fungo tossico che colpisce le colture ed è stato associato a decessi in scavi di tombe antiche. I ricercatori, guidati dall’Università della Pennsylvania (Stati Uniti), hanno modificato alcune delle loro molecole e le hanno testate contro le cellule leucemiche. Il risultato è stato un promettente composto contro il cancro che apre nuove frontiere nella scoperta di ulteriori farmaci derivati dai funghi. “I funghi ci hanno dato la penicillina. Ora questi nuovi risultati ci dimostrano che ci sono ancora molti farmaci derivati da prodotti naturali da scoprire”, sottolinea Sherry Gao, professore di bioingegneria all’Università della Pennsylvania e autore principale dello studio, i cui dettagli sono stati pubblicati lunedì sulla rivista Nature Chemical Biology. L’Aspergillus flavus, così chiamato per le sue spore gialle, è stato a lungo un microrganismo malvagio. Dopo che gli archeologi aprirono la tomba del re Tutankhamon negli anni ’20, una serie di morti premature tra il team di scavo diede origine alla maledizione del faraone. Decenni dopo, i medici hanno ipotizzato che le spore fungine, latenti per millenni, potessero aver giocato un ruolo importante. E negli anni ’70, una dozzina di scienziati entrarono nella tomba di Casimiro IV in Polonia, e la storia si ripeté: nel giro di poche settimane, dieci di loro morirono. Ulteriori ricerche rivelarono che la tomba conteneva A. flavus, le cui tossine possono causare infezioni polmonari. Ora, quello stesso fungo è la fonte inaspettata di una nuova e promettente terapia contro il cancro.
Una scoperta insolita
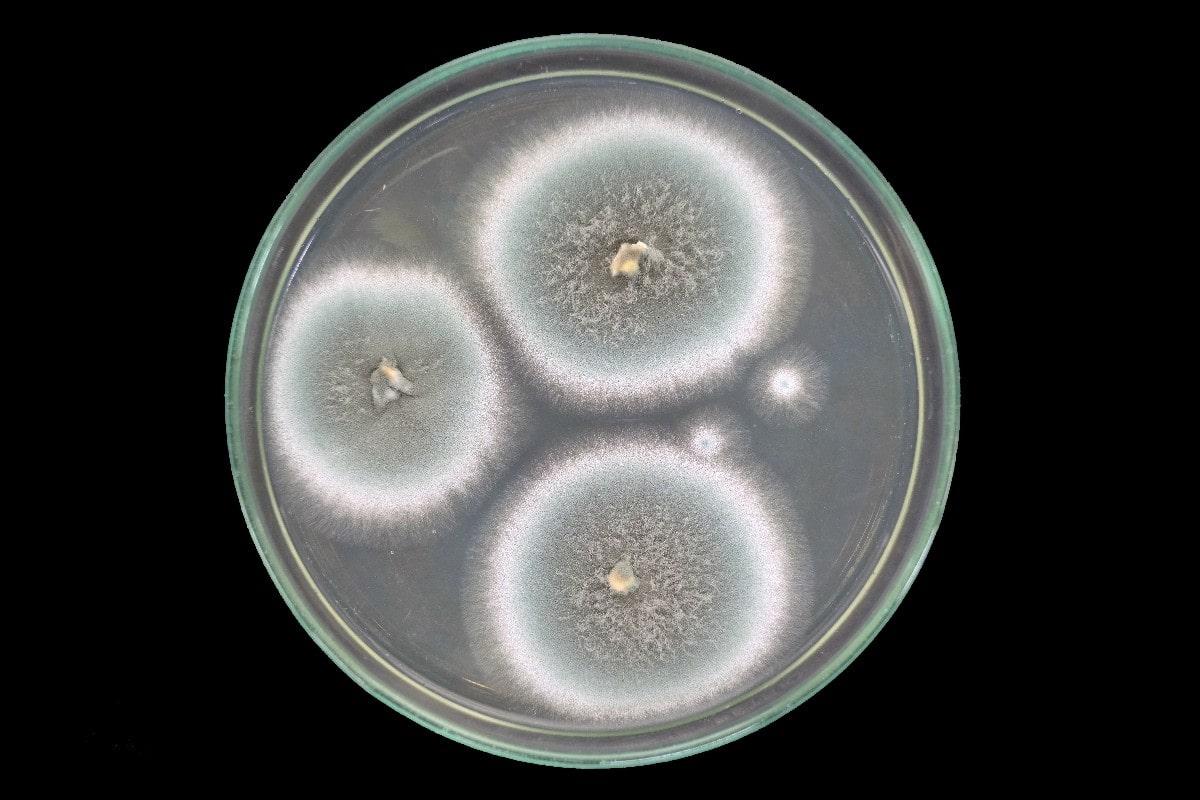
La terapia in questione è un tipo di peptidi sintetizzati dai ribosomi e modificati, o RiPP. Il nome fa riferimento al modo in cui il composto viene prodotto – dal ribosoma, una piccola struttura cellulare che produce proteine – e al fatto che viene successivamente modificato, in questo caso per migliorarne le proprietà antitumorali.
“Purificare queste sostanze chimiche è difficile”, spiega Qiuyue Nie, ricercatrice post-dottorato in Pennsylvania e prima autrice dell’articolo.
Sebbene siano stati identificati migliaia di RiPP nei batteri, solo pochi sono stati trovati nei funghi.
Per trovare i RiPP fungini, il team ha prima analizzato una dozzina di ceppi di Aspergillus, che secondo ricerche precedenti potrebbero contenere più di queste sostanze chimiche.
Confrontando le sostanze chimiche prodotte da questi ceppi con i componenti di base noti dei RiPP, i ricercatori hanno identificato l’A. flavus come un candidato promettente da studiare ulteriormente.
L’analisi genetica ha individuato una proteina specifica dell’A. flavus come fonte dei RiPP fungini. Quando i ricercatori hanno disattivato i geni che creano questa proteina, anche i marcatori chimici che indicavano la presenza dei RiPP sono scomparsi.
Questo nuovo approccio, che combina informazioni metaboliche e genetiche, non solo ha identificato la fonte dei RiPP fungini in A. flavus, ma potrebbe essere utilizzato per trovare altri RiPP fungini in futuro.
Un potente farmaco?

Dopo aver purificato quattro diversi RiPP, i ricercatori hanno scoperto che le molecole condividevano una struttura unica di anelli intrecciati che sono stati battezzati “asperigimicine”.
Anche senza modifiche, quando sono state mescolate con cellule tumorali umane, le asperigimicine hanno dimostrato il loro potenziale medico: due delle quattro varianti hanno avuto effetti potenti contro le cellule leucemiche.
Un’altra variante, alla quale i ricercatori hanno aggiunto un lipide presente anche nella pappa reale che nutre le api in fase di sviluppo, ha funzionato bene quanto la citarabina e la daunorrubicina, due farmaci approvati dalle autorità sanitarie statunitensi che da decenni sono utilizzati per trattare la leucemia.
Attraverso ulteriori esperimenti, i ricercatori hanno scoperto che le asperigimicine probabilmente interrompono il processo di divisione cellulare.
“Le cellule tumorali si dividono in modo incontrollato. Questi composti bloccano la formazione dei microtubuli, che sono essenziali per la divisione cellulare”, spiega Gao.
È importante sottolineare che i composti hanno avuto un effetto minimo o nullo sulle cellule tumorali del seno, del fegato o del polmone, né su una serie di batteri e funghi, il che suggerisce che gli effetti dirompenti delle asperigimicine sono specifici di determinati tipi di cellule, una caratteristica fondamentale per qualsiasi farmaco futuro.
Oltre a dimostrare il potenziale medico delle asperigimicine, i ricercatori hanno identificato gruppi simili di geni in altri funghi, suggerendo che ci sono ancora altri RiPPS fungini da scoprire.
Il prossimo passo è testare le asperigimicine su modelli animali, con la speranza di passare un giorno alla sperimentazione clinica sull’uomo.