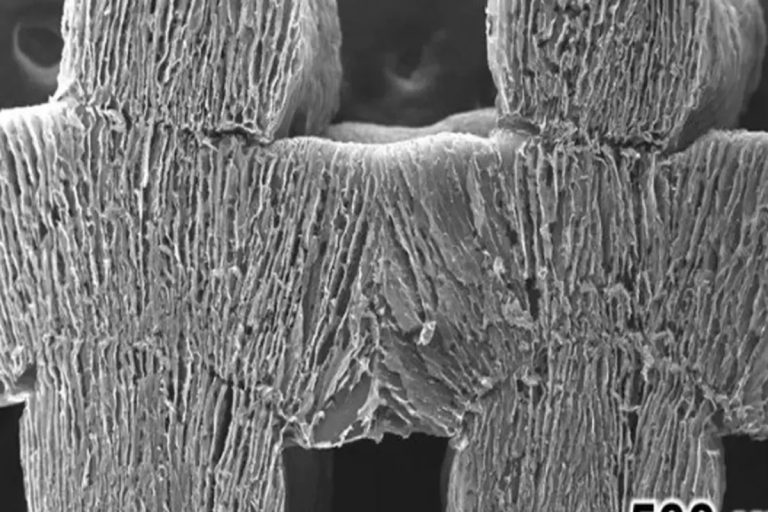
Una tossina temuta da decenni apre ora una finestra inaspettata verso nuove terapie oncologiche, grazie a una scoperta scientifica guidata dall’Università della Pennsylvania. Per quasi un secolo, il nome Aspergillus flavus ha evocato storie di mistero, malattia e morte. È stato indicato come il colpevole invisibile dietro la cosiddetta “maledizione del faraone”, dopo l’apertura della tomba di Tutankhamon nel 1922. Oggi, quello stesso fungo che un tempo era temuto negli scavi archeologici è stato trasformato dalla scienza in una speranza terapeutica per migliaia di pazienti. Un team interdisciplinare guidato da ricercatori dell’Università della Pennsylvania ha scoperto e modificato molecole di questo fungo tossico, trasformandole in composti in grado di distruggere le cellule tumorali con un’efficacia paragonabile a quella dei farmaci approvati dalla FDA per il trattamento della leucemia. Questa straordinaria scoperta, pubblicata di recente su Nature Chemical Biology, dimostra ancora una volta che il regno fungino, così spesso ignorato o temuto, nasconde un arsenale chimico dal potenziale terapeutico ancora inesplorato. “I funghi ci hanno dato la penicillina”, ricorda Sherry Gao, professore di ingegneria chimica e bioingegneria alla Penn e autore principale dello studio. “Questi risultati rivelano che ci sono ancora molti farmaci da scoprire nei prodotti naturali”.
Aspergillus flavus
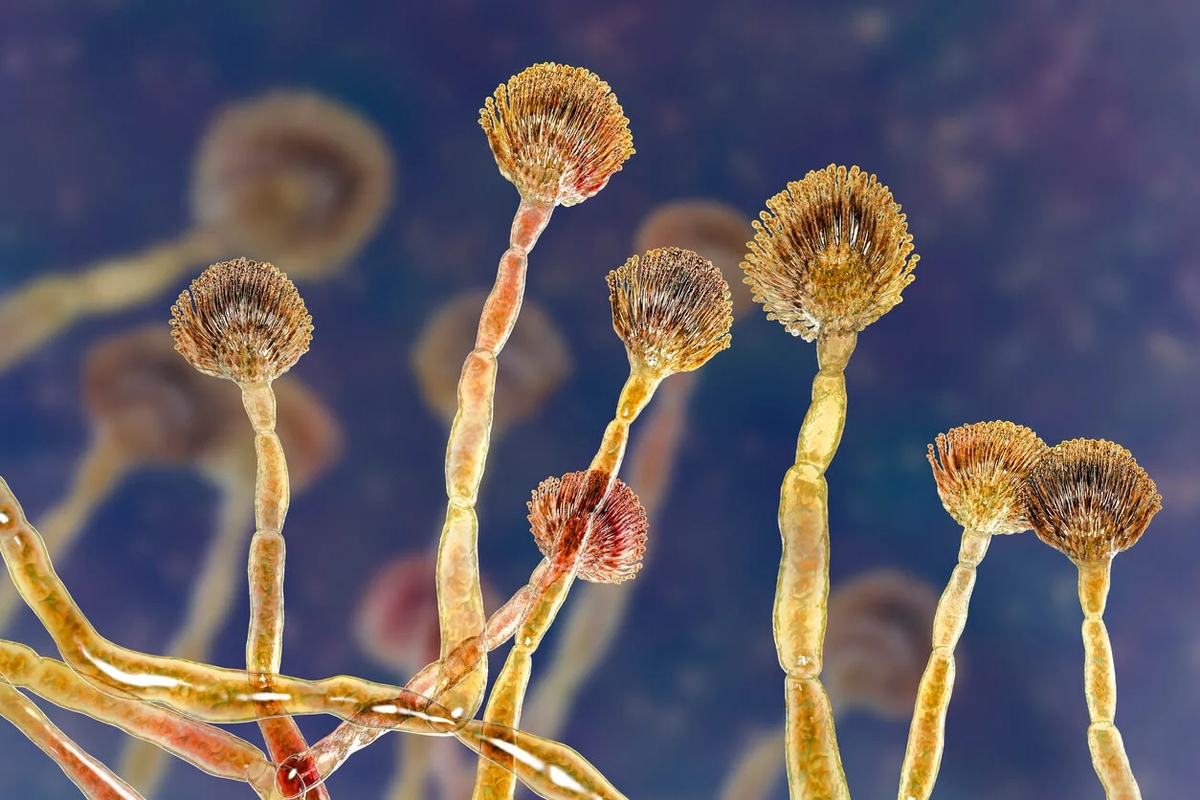
La storia dell’Aspergillus flavus inizia nelle profondità delle tombe reali e prosegue nei laboratori moderni. Dopo la misteriosa morte di diversi archeologi che avevano partecipato all’apertura della tomba di Tutankhamon, le teorie sulle spore millenarie hanno preso piede.
Decenni dopo, un incidente simile si verificò in Polonia: dei dodici scienziati che entrarono nella tomba del re Casimiro IV, dieci morirono nel giro di poche settimane. Il colpevole invisibile: lo stesso fungo, i cui metaboliti tossici possono causare infezioni polmonari letali in persone con un sistema immunitario compromesso.
Ma ora la narrazione ha preso una piega radicalmente diversa. Anziché essere una minaccia, l’A. flavus potrebbe diventare un’ancora di salvezza.
Il team di scienziati ha scoperto un tipo di composto chiamato RiPPs, acronimo inglese di peptidi sintetizzati ribosomiali e modificati post-traduzionalmente. Queste molecole, prodotte dal ribosoma cellulare e poi modificate chimicamente, erano state osservate principalmente nei batteri, ma quasi mai nei funghi.
Il fatto che siano state trovate nell’A. flavus cambia le regole del gioco. “La purificazione di questi composti è un processo complicato, ma è proprio questa complessità che conferisce loro una bioattività così notevole”, spiega Qiuyue Nie, primo autore dell’articolo.
I ricercatori hanno battezzato queste nuove molecole con il nome di asperigimicine, in onore del fungo da cui provengono. Sorprendentemente, due delle varianti estratte hanno mostrato attività antileucemica senza necessità di ulteriori modifiche. Un’altra variante, potenziata con un lipide simile a quello presente nella pappa reale delle api, ha dimostrato un’efficacia paragonabile a quella di farmaci classici come la citarabina e la daunorrubicina.
Questa modifica con lipidi non solo ha aumentato la potenza dell’asperigimicina, ma ha anche rivelato un meccanismo cellulare cruciale. Attivando o disattivando geni specifici nelle cellule leucemiche, i ricercatori hanno scoperto che uno di essi, l’SLC46A3, svolgeva un ruolo fondamentale: consentiva l’ingresso dei composti nel nucleo cellulare attraverso i lisosomi. “È come una porta d’accesso”, commenta Nie.
Questa scoperta potrebbe avere implicazioni che vanno oltre questa ricerca, facilitando l’ingresso di altri composti terapeutici simili.
Tumori con leucemia
Continuando gli studi, i ricercatori hanno osservato che le asperigimicine bloccavano la formazione dei microtubuli, strutture fondamentali nella divisione cellulare. Ciò è particolarmente rilevante nei tumori come la leucemia, dove le cellule si replicano in modo incontrollato.
Curiosamente, le asperigimicine non hanno mostrato effetti sulle cellule del cancro al seno, al fegato o al polmone, il che suggerisce una promettente specificità che potrebbe tradursi in trattamenti più mirati e meno tossici per il paziente.
Al di là della scoperta specifica, questo lavoro apre un nuovo capitolo nell’esplorazione dei farmaci fungini. I ricercatori hanno già identificato cluster genetici simili in altri funghi, il che indica un territorio ancora inesplorato. “Abbiamo solo scalfito la superficie”, dice Nie. “Ognuno di questi composti ha una storia da raccontare e un potenziale da rivelare”.
Il prossimo passo sarà testare le asperigimicine su modelli animali. Se i risultati saranno confermati, non è azzardato pensare a futuri studi clinici sull’uomo.